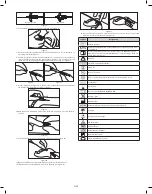
cathéter
radio-opaque
bouchon
de purge
interrupteur
FloSwitch
ergot de
pression
plateforme de sécurisation
aiguille avec
encoche
DESCRIPTION
Le cathéter artériel Merit RadialFlo™ est conçu pour accéder au système vasculaire afin
de prélever du sang et de surveiller la tension artérielle. Ce dispositif est équipé d’un
interrupteur FloSwitch qui permet de limiter les épanchements de sang ou de contrôler le
flux, selon le besoin. L’aiguille présente une encoche unique qui assure un retour sanguin
instantané dès la pénétration dans le vaisseau. Le cathéter radio-opaque permet une
visibilité à la radiographie et à la fluoroscopie.
UTILISATION PRÉVUE / MODE D’EMPLOI
Le cathéter artériel Merit RadialFlo™ est un dispositif qui s’insère dans le système
vasculaire du patient pour une utilisation de courte durée (moins de 30 jours) afin de
prélever du sang et de surveiller la tension artérielle. Le cathéter artériel Merit RadialFlo™
peut être utilisé sur tous les patients, en tenant compte de l’adaptation de l’anatomie
vasculaire et de la pertinence de la procédure.
PRÉCAUTION EN CAS DE RÉUTILISATION
Destiné à un usage unique. Ne pas réutiliser, ne pas retraiter, ne pas restériliser. La réutilisation,
le retraitement ou la restérilisation risqueraient de compromettre l’intégrité structurelle
du dispositif et/ou de provoquer une défaillance qui, à son tour, pourrait provoquer une
blessure, une maladie, voire le décès du patient. La réutilisation, le retraitement ou la
restérilisation pourraient également générer un risque de contamination du dispositif et/
ou provoquer une infection ou une infection croisée du patient, y compris, sans s’y limiter,
la transmission de maladie(s) infectieuse(s) d’un patient à un autre. La contamination du
dispositif pourrait provoquer une blessure, une maladie, voire le décès du patient.
CONTRE-INDICATION
Le dispositif RadialFlo™ est exclusivement destiné à la surveillance de la pression artérielle
et aux prélèvements de sang artériel. Ne pas utiliser pour l’administration artérielle de
perfusions intraveineuses.
AVANTAGES CLINIQUES
• Permet la surveillance de la pression artérielle
• Permet les prélèvements sanguins
AVERTISSEMENTS
• Apyrogène. Stérile. Ne pas utiliser si l’emballage est ouvert ou endommagé. Vérifier
l’intégrité de l’emballage individuel avant utilisation.
• Dispositif à usage unique. Éliminer le produit après usage. Ne pas restériliser. Une
réutilisation pourrait provoquer une infection ou une autre pathologie/lésion.
• Ne pas plier l’aiguille pendant l’utilisation du produit.
• Ne pas utiliser de ciseaux ou d’ustensiles tranchants au niveau ou à proximité du site
d’insertion afin d’éviter les coupures accidentelles du cathéter.
• Ne pas tenter de réinsérer dans le cathéter une aiguille partiellement ou
complètement retirée. En cas d’échec de la ponction artérielle, éliminer l’ensemble
du dispositif.
• Une exposition au sang, par suite d’une ponction percutanée avec une aiguille
contaminée ou par le biais des muqueuses, peut provoquer une maladie grave telle
que l’hépatite, le VIH, le SIDA ou toute autre pathologie infectieuse.
• Les médecins doivent connaître la technique d’accès artériel dite « au fil de l’aiguille ».
• Les médecins doivent connaître les complications associées au cathétérisme
artériel, comme l’ischémie artérielle, l’embolie gazeuse et la fragmentation du
cathéter qui nécessitent une procédure supplémentaire.
La législation fédérale des États-Unis stipule que ce produit ne doit être vendu
que par ou sur ordonnance d’un médecin.
PRÉCAUTIONS
• Le dispositif RadialFlo™ inséré dans les situations d’urgence dans lesquelles
la technique de stérilité pourrait être compromise doit être remplacé dans les
48 heures. Respecter les protocoles ou les procédures de l’hôpital/l’établissement
concernant la durée pendant laquelle le dispositif RadialFlo™ peut rester en place.
• La durée de vie du dispositif indiquée est de 96 heures, en fonction des
recommandations des Centres pour le contrôle et la prévention des maladies (CDC)
et de Joint Commission Intl (JCI) en termes de fréquence des remplacements.
• Vérifier que l’emplacement d’insertion du dispositif RadialFlo™ n’entrave pas le flux
collatéral jusqu’aux extrémités.
French
M O D E D ’ E M P L O I
RadialFlo
™
Cathéter artériel
• Éliminer immédiatement l’aiguille dans un conteneur pour objets tranchants
adéquat, tout de suite après son insertion.
• Signaler immédiatement les blessures par piqûre d’aiguille conformément au
protocole mis en place dans l’établissement.
INFORMATIONS DE SÉCURITÉ CONCERNANT LES IRM
Des études non cliniques ont démontré que le dispositif RadialFlo™ est compatible sous
conditions avec l’IRM. Un patient doté de ce dispositif peut être placé en toute sécurité
dans un système IRM dans les conditions suivantes :
• Champ magnétique statique de 1,5 tesla et 3 teslas, uniquement
• Gradient spatial maximum de champ magnétique de 2 000 gauss/cm (20 T/m)
• Système de RM maximum signalé, taux d’absorption spécifique (DAS) moyen du
corps entier de 2 W/kg pendant 15 minutes de balayage (c’est-à-dire par séquence
d’impulsions) dans le mode de fonctionnement normal
CONDITIONS DE STOCKAGE
Conserver dans un lieu frais et sec, à l’abri de la lumière directe du soleil.
CONSIGNES GÉNÉRALES
• Le cathéter artériel RadialFlo™ est disponible en une seule taille conformément aux
spécifications ci-dessous :
• Calibre : 20 G
• Diamètre extérieur standard : 1,10 mm
• Longueur standard : 45 mm
• Débit : 49 ml/min
• Pour une utilisation appropriée, les médecins doivent maîtriser le dispositif
RadialFlo™ et être formés à son utilisation.
• Respecter les précautions de contrôle des infections sur TOUS les patients.
• Une technique d’asepsie, une préparation correcte de la peau et une protection
continue du site d’insertion sont indispensables.
• Examiner fréquemment le site d’insertion du cathéter.
• Si des sutures sont utilisées pour maintenir en place le dispositif RadialFlo™, suturer
à travers les ouvertures de la plateforme de fixation plateforme de sécurisation.
• Ce produit ne contient pas les substances suivantes : DEHP, DIBP, DBP, BBP.
• Après utilisation, éliminer le dispositif conformément aux protocoles standards de
mise au rebut des déchets.
• Dans l’Union européenne, tout incident qui survient en relation avec le dispositif
doit être signalé au fabricant et à l’autorité compétente de l’État membre concerné.
MODE D’EMPLOI
1. Préparer le patient dans des conditions d’asepsie conformes à la politique et au
protocole hospitaliers.
2. Inspecter l’emballage pour vérifier qu’il n’est pas endommagé et que sa stérilité
est préservée. Se reporter aux flèches sur l’étiquette du dispositif pour ouvrir
l’emballage (voir la Figure 1).
Figure 1
3. Retirer le dispositif de son emballage (voir la Figure 2).
Figure 2
4. Retirer le capuchon de protection de l’aiguille en effectuant un mouvement de
traction rectiligne (voir la Figure 3).
Figure 3
5. Vérifier que l’interrupteur FloSwitch est en position ouverte appropriée avant
l’insertion de l’aiguille (voir la Figure 4).
4/52